Cosa sono gli aminoacidi?
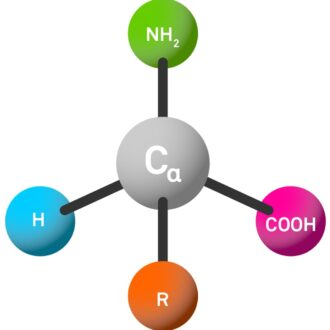
Gli aminoacidi più comuni in natura sono chiamati α-aminoacidi. Queste molecole hanno quattro diversi sostituenti attaccati all'atomo di carbonio centrale (chiamato atomo α-C):
Amino (NH₂, codice a tre lettere abbreviato come "H-").
Gruppo di acido carbossilico (COOH, abbreviato come "-OH" nel codice a tre lettere).
Catene laterali(R, che sono altamente variabili e determinano le proprietà degli aminoacidi e il peptide finale).
Atomo di idrogeno (H).
La connessione degli atomi α-C con questi quattro diversi gruppi dà proprietà chimiche uniche, che svolgono un ruolo chiave nel determinare il comportamento e le proprietà degli aminoacidi e dei peptidi.
Attività biologica degli aminoacidi
Gli aminoacidi possono presentare attività biologiche come:
Il triptofano (TRP) e l'acido glutammico (GLU) svolgono un ruolo chiave nei processi metabolici.
Il gruppo R (o la catena laterale) determina le proprietà uniche degli aminoacidi. Questi gruppi possono:
In termini semplici:Un atomo di idrogeno come la glicina (Gly).
Sono inclusi altri acidi: come acido aspartico (ASP) e acido glutammico (Glu).
Trasportare gruppi di base:Arginina (arg), lisina (Lys) o istidina (His).
Contiene gruppi polari: come serina (ser) o treonina (thr).
Idrocarburi non polari:Alanina (ALA), fenilalanina (PHE) o valina (Val).
Contenuto di zolfo:come si vede nella cisteina (CYS) e nella metionina (MET).
Il ruolo di L-aminoacidi e d-aminoacidi
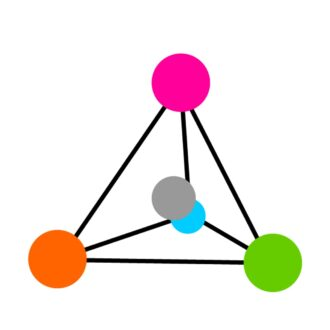
I quattro sostituenti dell'atomo α-C sono disposti agli angoli del tetraedro, con l'atomo α-C al centro (vedi Figura 3). Questa disposizione consente alle due forme di molecole di aminoacidi di esistere in forma specchio, simile alle mani sinistro e destro. Queste forme specchio sono note come "stereoisomeri" o "enantiomeri".
Importanza biologica degli enantiomeri
Sebbene gli enantiomeri abbiano proprietà chimiche e fisiche quasi identiche, i loro effetti biologici possono differire in modo significativo. La forma molecolare è fondamentale per la sua interazione con obiettivi biologici. Un enantiomero può legarsi efficacemente al bersaglio, un altro potrebbe non essere o in alcuni casi avere un effetto negativo. In soluzione, l'enantiomero ruota il piano leggero polarizzato nella direzione opposta.
Tempo post: 2025-09-05
